Le Brésil est le plus grand producteur mondial de niobium et détient environ 98 pour cent des réserves actives de la planète.Cet élément chimique est utilisé dans les alliages métalliques, en particulier dans l'acier à haute résistance, et dans une gamme presque illimitée d'applications de haute technologie, depuis les téléphones portables jusqu'aux moteurs d'avion.Le Brésil exporte la majeure partie du niobium qu’il produit sous forme de produits tels que le ferroniobium.
Une autre substance que le Brésil possède également en grande quantité mais sous-utilisée est le glycérol, un sous-produit de la saponification des huiles et des graisses dans l'industrie du savon et des détergents, et des réactions de transestérification dans l'industrie du biodiesel.Dans ce cas, la situation est encore pire car le glycérol est souvent jeté comme déchet et l’élimination appropriée de gros volumes est complexe.
Une étude réalisée à l'Université fédérale de l'ABC (UFABC) dans l'État de São Paulo, au Brésil, a combiné le niobium et le glycérol dans une solution technologique prometteuse pour la production de piles à combustible.Un article décrivant l’étude, intitulé « Le niobium améliore l’activité électrocatalytique du Pd dans les piles à combustible alcalines directes au glycérol », est publié dans ChemElectroChem et fait la couverture de la revue.
« En principe, la cellule fonctionnera comme une batterie alimentée au glycérol pour recharger de petits appareils électroniques tels que des téléphones portables ou des ordinateurs portables.Il peut être utilisé dans les zones non couvertes par le réseau électrique.Plus tard, la technologie pourra être adaptée pour faire fonctionner des véhicules électriques et même pour alimenter les maisons en électricité.Les applications potentielles sont illimitées à long terme », a déclaré le chimiste Felipe de Moura Souza, premier auteur de l'article.Souza bénéficie d'une bourse de doctorat directe de la Fondation de recherche de São Paulo (FAPESP).
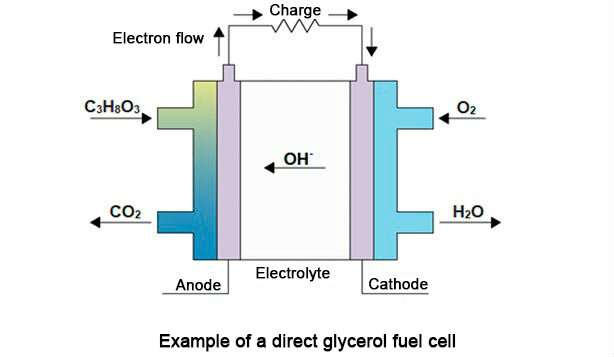
Dans la cellule, l'énergie chimique provenant de la réaction d'oxydation du glycérol dans l'anode et de la réduction de l'oxygène de l'air dans la cathode est convertie en électricité, ne laissant que du carbone et de l'eau comme résidus.La réaction complète est C3H8O3 (glycérol liquide) + 7/2 O2 (oxygène gazeux) → 3 CO2 (gaz carbonique) + 4 H2O (eau liquide).Une représentation schématique du processus est présentée ci-dessous.
« Le niobium [Nb] participe au processus en tant que co-catalyseur, aidant l'action du palladium [Pd] utilisé comme anode de la pile à combustible.L'ajout de niobium permet de réduire de moitié la quantité de palladium, diminuant ainsi le coût de la cellule.En même temps, cela augmente considérablement la puissance de la cellule.Mais sa principale contribution est une réduction de l'empoisonnement électrolytique du palladium qui résulte de l'oxydation d'intermédiaires fortement adsorbés lors du fonctionnement à long terme de la cellule, comme le monoxyde de carbone », a déclaré Mauro Coelho dos Santos, professeur à l'UFABC. , directeur de thèse pour le doctorat direct de Souza et chercheur principal de l'étude.
Du point de vue environnemental, qui doit plus que jamais être un critère déterminant dans les choix technologiques, la pile à combustible au glycérol est considérée comme une solution vertueuse car elle peut remplacer les moteurs à combustion alimentés par des énergies fossiles.
Heure de publication : 30 décembre 2019